Введение в прибор для измерения растворенного кислорода

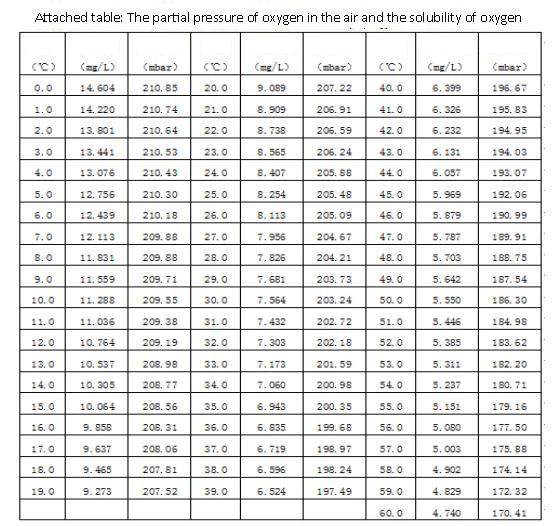
Растворенный кислород — это количество кислорода, растворенного в воде, обычно обозначаемое как DO, выраженное в миллиграммах кислорода на литр воды (в мг/л или ppm). Некоторые органические соединения подвергаются биодеградации под действием аэробных бактерий, которые потребляют растворенный кислород в воде, и его запасы не восполняются вовремя. Анаэробные бактерии в водоеме быстро размножаются, и органические вещества вызывают почернение воды из-за загрязнения и неприятного запаха. Количество растворенного кислорода в воде является показателем способности водоема к самоочищению. Если растворенный кислород потребляется и быстро восстанавливается до исходного уровня, это указывает на сильную способность водоема к самоочищению или на незначительное загрязнение. В противном случае это означает, что водоем серьезно загрязнен, способность к самоочищению слабая или даже утрачена. Это тесно связано с парциальным давлением кислорода в воздухе, атмосферным давлением, температурой воды и ее качеством.
1. Аквакультура: обеспечение потребности водных организмов в кислороде, мониторинг содержания кислорода в режиме реального времени, автоматическая сигнализация, автоматическая оксигенация и другие функции.

2. Мониторинг качества природных водоемов: определение степени загрязнения и способности воды к самоочищению, а также предотвращение биологического загрязнения, такого как эвтрофикация водоемов.
3. Очистка сточных вод, контрольные показатели: для контроля эффективности очистки воды используются показатели анаэробного резервуара, аэробного резервуара, аэрационного резервуара и другие.

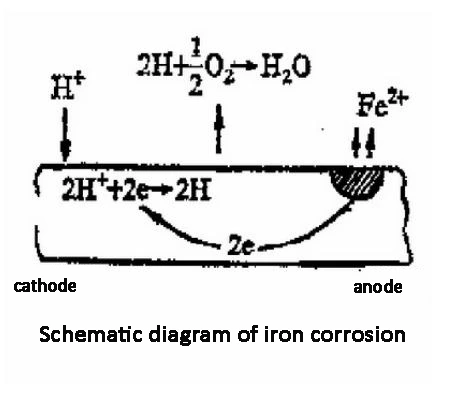
4. Контроль коррозии металлических материалов в промышленных водопроводных трубопроводах: Как правило, для контроля содержания кислорода в трубопроводе и предотвращения коррозии используются датчики с диапазоном ppb (мкг/л). Они часто применяются на электростанциях и в котельном оборудовании.
В настоящее время наиболее распространенный на рынке измеритель растворенного кислорода использует два принципа измерения: мембранный метод и флуоресцентный метод. В чем же разница между ними?
1. Мембранный метод (также известный как полярографический метод, метод постоянного давления)
Мембранный метод основан на электрохимических принципах. Полупроницаемая мембрана используется для отделения платинового катода, серебряного анода и электролита от внешней среды. Обычно катод находится практически в непосредственном контакте с этой пленкой. Кислород диффундирует через мембрану в соотношении, пропорциональном его парциальному давлению. Чем выше парциальное давление кислорода, тем больше кислорода проходит через мембрану. Когда растворенный кислород непрерывно проникает через мембрану и попадает в полость, он восстанавливается на катоде, генерируя ток. Этот ток прямо пропорционален концентрации растворенного кислорода. Прибор подвергается процессу усиления для преобразования измеренного тока в единицу концентрации.

2. Флуоресценция
Флуоресцентный зонд имеет встроенный источник света, излучающий синий свет и освещающий флуоресцентный слой. После возбуждения флуоресцентное вещество излучает красный свет. Поскольку молекулы кислорода могут отнимать энергию (эффект тушения), время и интенсивность возбужденного красного света связаны с концентрацией молекул кислорода. Концентрация обратно пропорциональна. Измеряя разность фаз между возбужденным красным светом и эталонным светом и сравнивая ее с внутренним калибровочным значением, можно рассчитать концентрацию молекул кислорода. Во время измерения кислород не расходуется, данные стабильны, результаты надежны, и отсутствуют помехи.
Давайте проанализируем это с точки зрения использования для всех:
1. При использовании полярографических электродов перед калибровкой или измерением необходимо прогреть их в течение как минимум 15-30 минут.
2. Из-за потребления кислорода электродом концентрация кислорода на поверхности зонда мгновенно снижается, поэтому важно перемешивать раствор во время измерения! Другими словами, поскольку содержание кислорода измеряется путем потребления кислорода, возникает систематическая ошибка.
3. Вследствие протекания электрохимической реакции концентрация электролита постоянно снижается, поэтому необходимо регулярно добавлять электролит для поддержания его концентрации. Для предотвращения образования пузырьков в электролите мембраны необходимо удалять воздух из всех жидких камер при установке головки мембраны.
4. После добавления каждого электролита требуется новый цикл калибровки (обычно калибровка нулевой точки в бескислородной воде и калибровка наклона на воздухе), и даже если используется прибор с автоматической температурной компенсацией, калибровка должна быть близка к оптимальной. Лучше калибровать электрод при температуре раствора образца.
5. В процессе измерения на поверхности полупроницаемой мембраны не должно оставаться пузырьков, иначе она будет восприниматься как образец, насыщенный кислородом. Не рекомендуется использовать ее в аэрационном резервуаре.
6. Из-за технологических особенностей мембранная головка относительно тонкая, особенно легко повреждается в определенных агрессивных средах и имеет короткий срок службы. Это расходный материал. В случае повреждения мембрану необходимо заменить.
В заключение, следует отметить, что мембранный метод характеризуется высокой точностью, коротким сроком технического обслуживания и большими трудностями в эксплуатации!
А что насчет флуоресцентного метода? Благодаря физическому принципу, кислород используется только в качестве катализатора в процессе измерения, поэтому процесс измерения практически свободен от внешних помех! Высокоточные, не требующие обслуживания и более качественные зонды, как правило, остаются без присмотра в течение 1-2 лет после установки. Действительно ли у флуоресцентного метода нет недостатков? Конечно, есть!






